 Исследователь в Массачусетской больнице общего профиля создал искусственную конечность крысы. Полученный образец отвечает на внешние раздражители и имеет функционирующие кровеносные сосуды. Результат выглядит как ампутированная конечность размером чуть меньше человеческого пальца, хотя на самом деле она была создана искусственным путём. Следующим может стать эксперимент с участием конечности примата.
Исследователь в Массачусетской больнице общего профиля создал искусственную конечность крысы. Полученный образец отвечает на внешние раздражители и имеет функционирующие кровеносные сосуды. Результат выглядит как ампутированная конечность размером чуть меньше человеческого пальца, хотя на самом деле она была создана искусственным путём. Следующим может стать эксперимент с участием конечности примата.По всему миру живёт огромное количество инвалидов. Только в США ампутантов 2 миллиона. Сегодня с частью проблем могут справиться протезы. Но они выглядят неестественно и технологически далеки от того, чем грезят авторы киберпанковых произведений. Другим вариантом может быть трансплантация конечностей. В этом случае крупным минусом является необходимость употребления иммунодепресантов на протяжении всей оставшейся жизни — иначе организм отвергнет чужеродную вставку. У созданной в лаборатории конечности этих недостатков нет. Результат содержит клетки только реципиента. Выращенная конечность может выглядеть и функционировать так же, как и утерянная, но она не требует подавления иммунитета.
Для выращивания лапки торакальному хирургу Харальду Отту требуются недели. Он удовлетворяет все её необходимости, пока она растёт в специальном инкубаторе. Используется техника «децеллюляризация/рецеллюляризация» (decel/recel). Метод состоит из следующих шагов: орган мёртвого донора очищается от клеток, от него остаётся только мёртвая основа из инертного коллагена и других веществ. Затем остов населяется нужными клетками из тканей реципиента. В биореакторе происходит подпитывание и рост тканей. Поскольку клеток донора в полученном органе нет, он не будет отвергнут иммунной системой реципиента.
То есть децеллюляризация/рецеллюляризация — это не полное создание с нуля. Ранее эта техника уже использовалась для выращивания органов с различной степенью успеха. Отличие лапки от относительно простых синтетических мочевых пузырей или трахей состоит в большом разнообразии тканей: это кровеносные сосуды, нервные окончания, мускулы и кости. Ткани имеют разные структуры и функции.
В данном случае процесс начинался с мёртвой конечности крысы. Процесс децеллюрязации проходил так же, как и в исследованиях с внутренними органами. В сосудистую систему мёртвой передней конечности был введён специальный раствор-очиститель. Он удалил все клеточные материалы, оставляя сосудистую сеть и нервную матрицу. Процесс удаления остатков клеток занял неделю. В результате была получена бесклеточная структура, которая служила основой для разнообразных тканей конечности.
Затем остов был помещён в биореактор. В коллагеновую артерию была подключена искусственная система циркуляции, снабжавшая конечность питательными веществами и кислородом. Чтобы усилить структуру кровеносных сосудов для предстоящей для них нагрузки, в них были введены клетки человеческого эндотелия. Отт населил структуры лапки крысы клетками реципиента. В полости ранее бывшей мускулами структуры ввели миобласты, клетки, которые вырастают в мышцы. Через пять дней начала проводиться стимуляция развития мускулов с помощью электрических импульсов. Всего для роста кровеносных сосудов и мускулов потребовалось 3 недели. Отт закончил процесс пересадкой кожи.
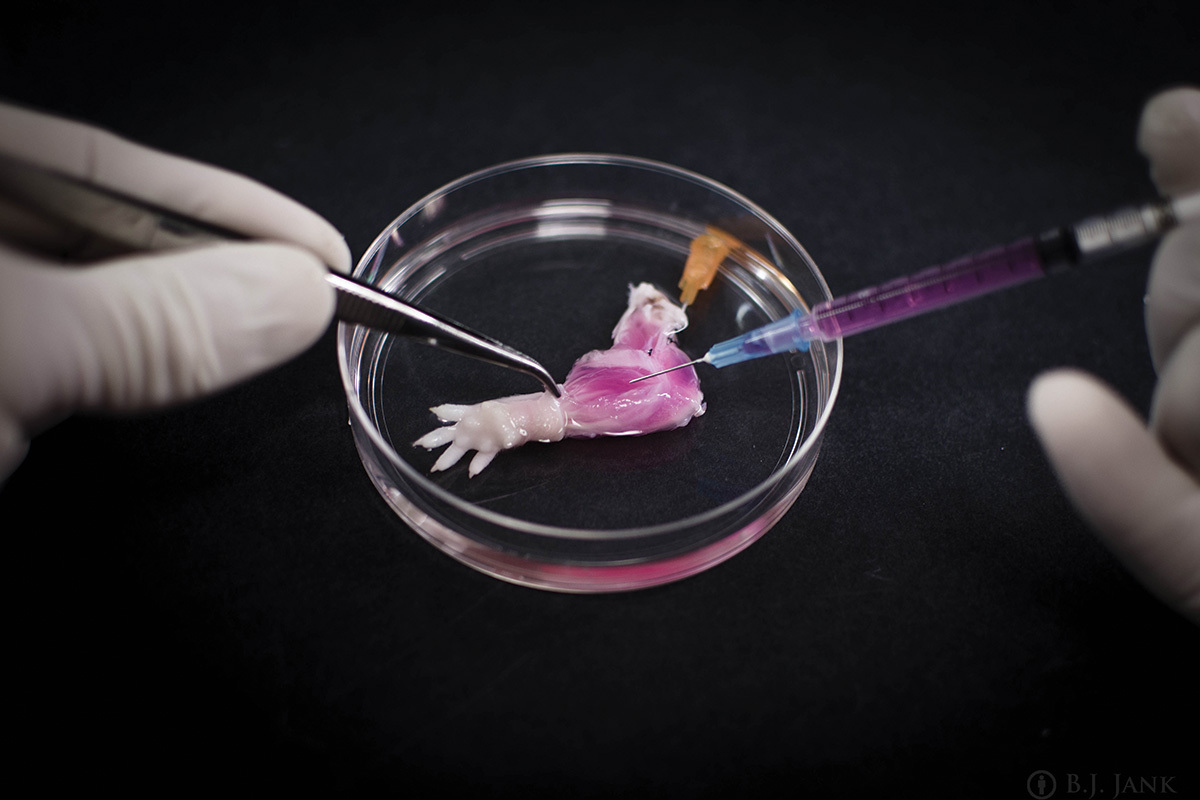
B J Jank, Ott Laboratory
Для проверки работоспособности мускулов выращенной лапки исследователи использовали электрические импульсы. Конечность могла сгибаться и разгибаться с силой в 80 % от силы мышц новорождённого. Клетки были ориентированы в корректном направлении мышечных волокон. Также выращенные конечности присоединялись к здоровым крысам под наркозом. В этом случае был продемонстрирован успешный кровеносный поток. Не проводились проверки на движения мышц и на отторжение тканей. Всего было децеллюрязировано порядка 100 конечностей крыс, более половины были рецеллюрязированы.
Отт замечает, что для исследователей ещё много работы. Конечность требуется снабдить костными структурами, хрящами и другими типами клеток. Нужно убедиться, что они тоже могут быть восстановлены. Затем нужно показать развитие нервной системы. Результаты пересадки донорских кистей рук показывают, что нервы реципиента проникают в новый орган, постепенно позволяя управлять им. Важно проверить, происходит ли то же самое в выращиваемых конечностях.
Также Отт и его коллеги смогли продемонстрировать децеллюляризацию конечности бабуина (на фотографии ниже). Команда исследователей начала населять получившийся остов человеческими клетками кровеносных сосудов. Далее будет проводиться ввод миобластов человека для выращивания мышц. Но Отт предупреждает, что до первых конечностей для тестов на людях потребуется как минимум десятилетие. Возможно, в отдалённом будущем любой желающий сможет пожертвовать после смерти свои руки и ноги для выращивания конечностей для инвалидов.
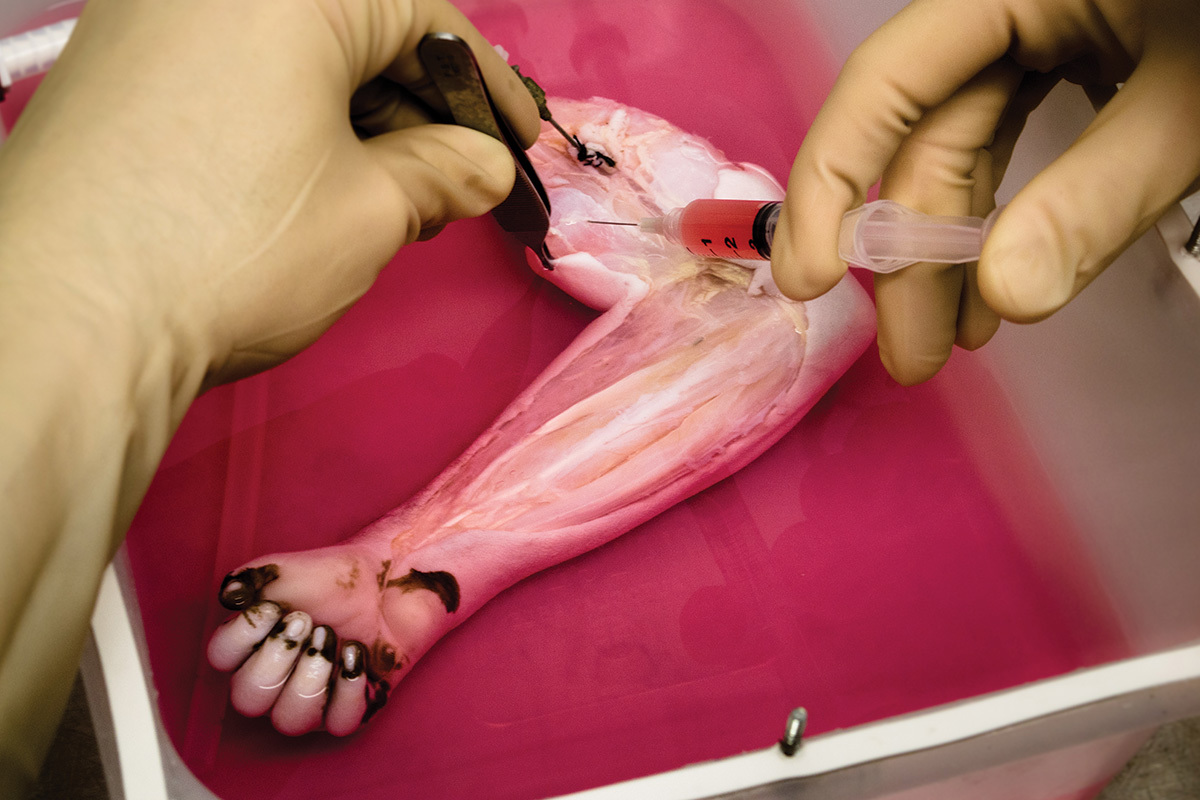
B J Jank, Ott Laboratory
Стив Бадылак из Питтсбургского университета рассказал о возможных проблемах, которые будут стоять перед командой Отта. Наибольшие трудности может вызывать циркуляция в сосудах: эндотелий не должен закупоривать мельчайшие капилляры. Оскар Ашманн из Венского медицинского университета заявил, что в таком сложном органе, как рука, слишком много разных тканей и структур, поэтому децеллюляризация/рецеллюляризация не сможет стать реальным процессом выращивания потерянных конечностей. Чтобы рука выполняла хоть какую-либо полезную функцию, она должна стимулироваться тысячами нервов. Сейчас проблемы с нервной тканью — это непреодолимый барьер, говорит Ашманн.
По материалам New Scientist, Washington Post и новостного сайта Массачусетской больницы общего профиля. doi.org/4w7.









